Anvisa autoriza mudanças em teste da “vacina de Oxford”
A alteração é a aplicação de uma dose de reforço, totalizando duas doses em vez de uma, como originalmente havia sido proposto
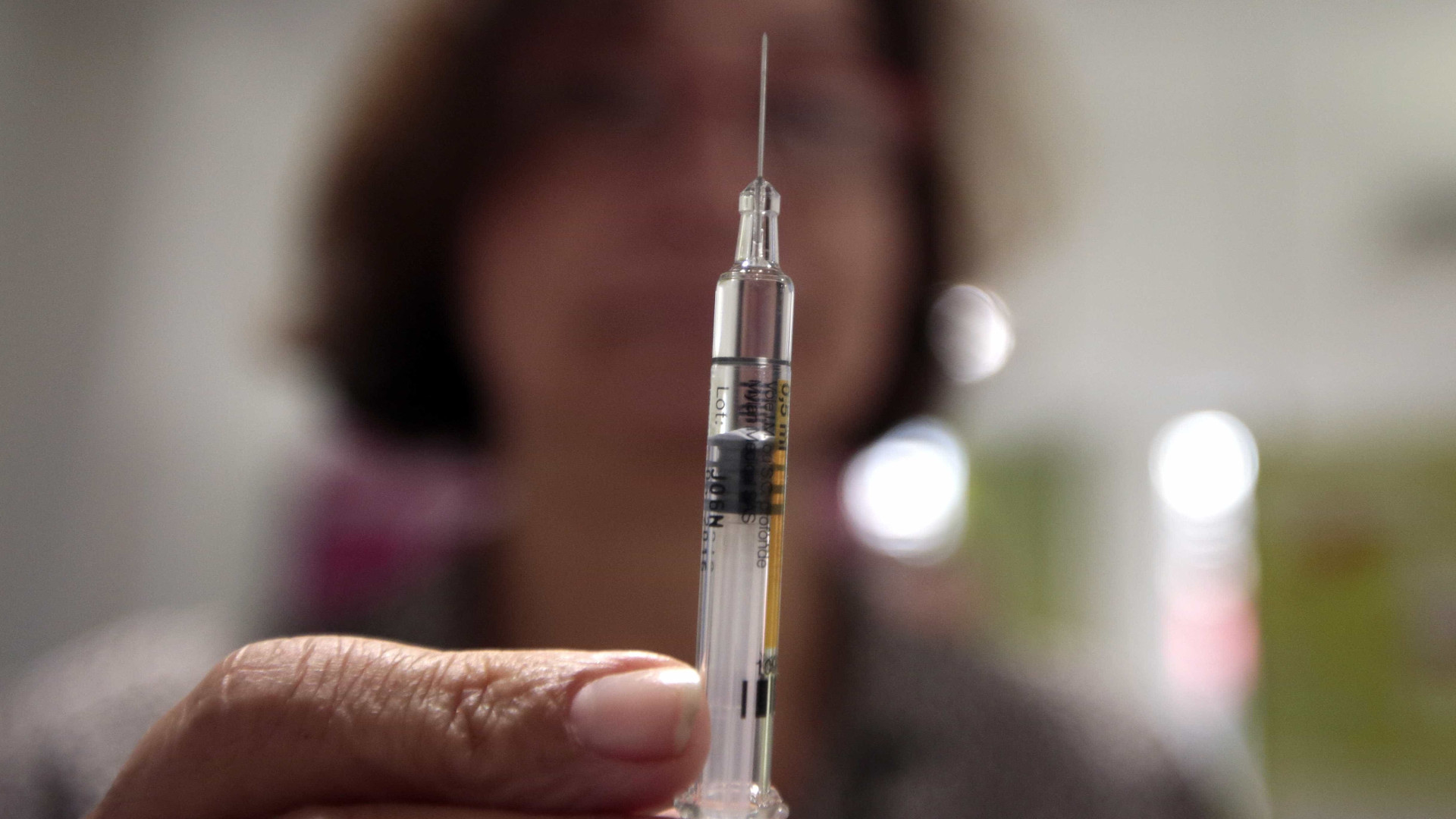
© Reuters

Brasil Pandemia
A Agência Nacional de Vigilância Sanitária (Anvisa) autorizou mudanças no protocolo do teste com a chamada “vacina de Oxford”, objeto de um dos ensaios clínicos em curso no Brasil e apontada por pesquisadores e pelo governo federal como uma das alternativas mais promissoras de prevenção da covid-19.
A alteração é a aplicação de uma dose de reforço, totalizando duas doses em vez de uma, como originalmente havia sido proposto. Essa parcela adicional de vacina será ministrada tanto para os que já haviam recebido a substância quanto para os voluntários que ainda receberão a vacina. No primeiro caso, o intervalo entre uma e outra será de quatro semanas.
A medida foi tomada a pedido dos responsáveis pela pesquisa. A mudança se deve ao fato de alguns estudos indicarem que a aplicação de duas doses pode produzir resultados mais efetivos na imunização.
Outra atualização foi a ampliação da faixa etária do grupo participante da pesquisa. Originalmente eram admitidas pessoas de 18 a 55 anos. A idade limite foi estendida para até 69 anos, incluindo uma faixas de idosos, o segmento que mais morre em função da covid-19.
A “vacina de Oxford” passou a ser conhecida popularmente por este apelido por se tratar de uma pesquisa capitaneada pela Universidade de Oxford, no Reino Unido, em parceria com o laboratório Astrazeneca.
O governo brasileiro celebrou um acordo com os agentes responsáveis para que o Brasil tenha preferência na aquisição de insumos e da transferência de tecnologia. O acerto inclui a pré-compra de insumos para 30 milhões de doses em dezembro e o repasse de tecnologia para a fabricação no país de mais 70 milhões de doses ao longo do ano de 2021.
A produção ficará a cargo da Fundação Oswaldo Cruz (Fiocruz), órgão vinculado ao Ministério da Saúde.
Na semana passada, o governo federal editou Medida Provisória alocando R$ 1,99 bilhão em recursos para o custeio da aquisição dos insumos e transferência de tecnologia da vacina.
Desenvolvida pela Universidade de Oxford, a vacina foi elaborada através da plataforma tecnológica de vírus não replicante (a partir do adenovírus de chimpanzé, obtém-se um adenovírus geneticamente modificado, por meio da inserção do gene que codifica a proteína S do vírus SARS-COV-2, do novo coronavírus). De acordo com o governo, embora seja baseada em uma nova tecnologia, esta plataforma já foi testada anteriormente para outras doenças, como, por exemplo, nos surtos de ebola e Mers (síndrome respiratória do Oriente Médio causada por outro tipo de coronavírus) e é semelhante a outras plataformas da Bio-Manguinhos/Fiocruz, o que facilita a sua implantação em tempo reduzido. A vacina está na Fase 3 dos ensaios clínicos, que é a última etapa de testes em seres humanos para determinar a segurança e eficácia.

 PORTUGAL
PORTUGAL